汪貽廣團隊發展納米藥物細胞內生物利用度定量新策略
2021年4月22日,國際權威期刊Nature子刊《Nature Communications》在線刊登了意昂2平台藥學院天然藥物及仿生藥物國家重點實驗室汪貽廣研究團隊的最新研究成果“Quantitative imaging of intracellular nanoparticle exposure enables prediction of nanotherapeutic efficacy”。

近年來,納米藥物在癌症治療中發揮越來越重要的作用。然而,癌症患者的腫瘤異質性使得同一種納米藥物在不同腫瘤類型甚至同種類型不同個體間均表現出較大治療響應差異,低響應性亞群掩蓋了整體治療效果,導致納米藥物的臨床轉化成功率較低🌆👺。傳統的定量方法只能提供納米藥物的宏觀組織分布,而不能區分細胞內攝取的納米藥物與細胞外及血管中分布的納米藥物🉐。越來越多的證據表明:納米載體的細胞攝取及其胞內轉運途徑對於細胞內靶點的藥物生物利用度及藥效發揮具有決定性作用。因此,發展新型智能遞送技術,解析納米藥物在活體動物的細胞內外分布與細胞內攝取效率,進而對癌症病人進行篩選,實現個體化治療具有重要的臨床指導意義🌹。
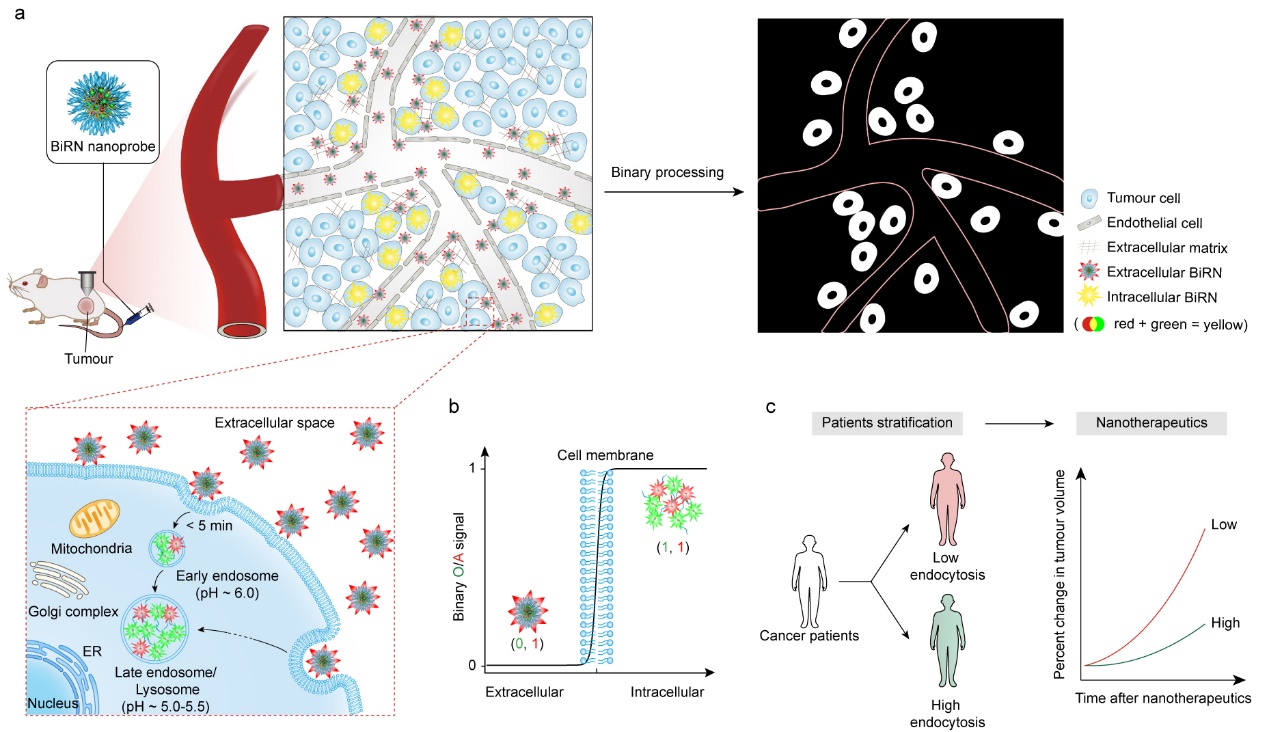
基於以上科學問題,汪貽廣研究團隊以內吞過程中pH值下降為響應信號設計並構建了一種二元比率成像納米探針(BiRN),它由“常亮式”熒光模塊和“關-開”熒光模塊構成🫦。靜脈註射後,“關-開”熒光模塊在血液和腫瘤細胞外間隙液(pHe ~ 6.5-6.8)中保持“關閉”;當納米藥物被細胞攝取進入到早期內涵體(pH ~ 6.0)後,“關-開”熒光模塊信號迅速“打開”,報告納米藥物“內吞事件”的發生;而在整個體內過程中,“常亮式”熒光模塊的熒光信號保持不變🦚。通過二進製比率數據處理,腫瘤血管及細胞外分布的納米粒信號被完全消除,從而實現對活體動物腫瘤內納米藥物的動態內吞效率和內吞量的定量化成像。采用該項技術,我們首次發現:① 靜脈註射24 h,10.7-28.2%的腫瘤蓄積納米粒被腫瘤細胞及相關細胞攝取,並且不同類型腫瘤的內吞效率具有很大差異;②以腫瘤內納米粒的細胞內吞量代替腫瘤內納米粒蓄積量(EPR效應)對腫瘤病人進行分級和抗腫瘤效應進行預測,具有更好的相關性🫳。該項研究為評估新型納米藥物的腫瘤靶向性和癌症患者分級及個性化治療提供了有力的工具。
汪貽廣研究員為本研究論文的通訊作者,博士研究生殷晴晴為論文的第一作者。該項研究得到了科技部重點研發計劃、國家自然科學基金和北京市自然基金傑出青年科學基金等的資助。

左起:殷晴晴(博士研究生)、汪貽廣(研究員)
原文鏈接:https://www.nature.com/articles/s41467-021-22678-z
作者簡介:

汪貽廣,博士,意昂2平台研究員、博士生導師,藥學院藥劑學系主任🗡、天然藥物及仿生藥物國家重點實驗室課題組長,入選中組部高層次人才。主要從事智能納米藥物遞送及疾病診療研究,取得了一系列創新性成果,以第一作者或通訊作者在Nat.Mater.💁🏽♂️、Nat. Commun.、Angew. Chem. Int. Ed.、Adv. Mater.、Adv. Funct. Mater.、Adv. Sci.、Nano Lett.等國際著名期刊上發表SCI學術論文50余篇。作為負責人獲得國家自然科學基金“優秀青年科學基金”🪻、北京市自然基金“傑出青年科學基金”、國家重點研發計劃等資助。先後獲得2015年中國藥學會-中恒青年藥劑學獎、2017年中國藥學會-賽諾菲青年生物藥物獎。目前擔任中國藥學會藥劑學專委會委員、中國藥學會納米藥物專委會委員等🫙。
(藥學院)
編輯:玉潔


